Thiamine (vitamine B1)
Date de dernière édition : 22/09/2024
La thiamine (vitamine B1) est le premier composé reconnu comme vitamine, substance indispensable au métabolisme et dont le corps dépend d'apports extérieurs. Elle est nécessaire pour l'être humain au bon fonctionnement des systèmes neurologique, musculaire (y compris cardiaque), digestif et du métabolisme glucidique. Les situations de carences sont fréquentes (le plus souvent dans un contexte d'éthylisme chronique dans les pays développés) et susceptibles d'induire des pathologies sévères.
Nature et propriétés chimiques
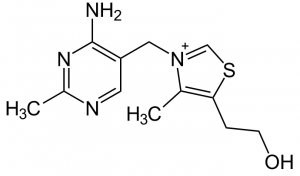
La thiamine est une molécule hydrosoluble et non soluble dans l'acétone. Elle est thermolabile (dénaturation à 100°C en milieux aqueux et alcalins). Elle se présente sous forme de cristaux dans des conditions standards.
Elle comprend un noyau pyrimidique et un noyau thiazolique. Se présentant sous forme de chlorhydrate ou de mononitrate, sa formule brute est C12H17N4OS+.
Eléments de physiopathologie
Le corps humain est incapable de produire la thiamine et dépend des apports alimentaires. Elle n'est stockée qu'en très faibles quantités par les muscles, le système nerveux et le foie. En l'absence d'apports extérieurs suffisant, ces réserves s'épuisent en 2 à 3 semaines.
La thiamine est le précurseur de deux formes bio-actives nécessaires au bon déroulement de plusieurs voies métaboliques :
- La thiamine pyrophosphate (ou diphosphate de thiamine, TPP) intervenant notamment dans :
- Métabolisme glucidique et production de réserves d'énergie :
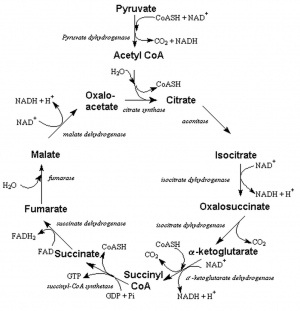
- Cycle de Krebs : le TPP catalyse les décarboxylations oxydatives du pyruvate participant à la production d'acétyl-CoA et de l'alpha-ketoglutarate participant à la formation de succinyl-CoA.
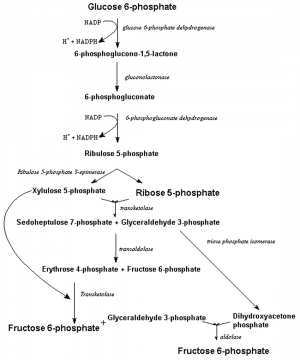
- Voie des pentoses phosphates : le TPP est également le co-enzyme de la transketolase catalysant la production de fructose-6-phosphate
- Dégradation du pyruvate (cf cycle de Krebs) dont l'accumulation conduit à une surproduction de lactates (toxiques pour toutes les cellules, mais en particulier pour les neurones et cellules gliales)
- La décarboxylation oxydative du pyruvate (cf cycle de Krebs) est également une étape nécessaire à la formation d'acétylcholine (neurotransmetteur) et celle de l'alpha-ketoglutarate à la formation d'acide gamma-aminobutirique (GABA, neurotransmetteur)
- Métabolisme glucidique et production de réserves d'énergie :
- La thiamine triphosphate dont le rôle est encore mal connu. Elle serait impliquée dans les processus de signalisation cellulaire et de neurotransmission.
Le magnésium est un co-facteur indispensable à l'activité de la TPP.
Une insuffisance en TPP ou ses co-facteurs entraîne donc une souffrance cellulaire (insuffisance énergétique), particulièrement pour le système nerveux et le muscle cardiaque (tissus les plus demandeurs en énergie). Certains auteurs évoquent une possible susceptibilité génétique (anomalies enzymatiques dans les voies sus-mentionnées) individuelle.
Une telle insuffisance peut survenir dans différentes situations (isolées ou combinées) :
- Apports alimentaires en thiamine insuffisants
- Défaut de l'absorption intestinale de la thiamine
- Défaut de phosphorylation de la thiamine en TPP
- Situations hypermétaboliques et hypercataboliques physiologiques ou pathologiques (surconsommation de TPP)
- Excrétion urinaire accrue de thiamine
- La présence de composés neutralisant la thiamine (thiaminases)
- Hypomagnésémie sévère
Sources alimentaires et besoins journaliers
Les sources alimentaires de thiamine sont principalement : viande de boeuf, levure, haricots, lentilles, noix, avoine, riz non raffiné, graines, blé et céréales à grains entiers, oranges, lait et dérivés, oeufs.
Les besoins journaliers chez l'adulte dans des conditions normales sont estimés à 0,5 à 2 mg/ jour.
Implications cliniques
Etiologie des carences et des troubles du métabolisme de la thiamine
- Dans les pays en voie de développement : la sous-alimentation et la malnutrition en sont considérées comme les causes quasi-exclusives. Les données épidémiologiques sont cependant pauvres.
- Dans les pays développés :
- L'alcoolisme chronique en est la cause largement prédominante (présent dans > 50% des cas)
- mécanismes possibles : ingestats alimentaires fréquemment inadéquats chez les éthyliques, troubles de l'absorption intestinale dus à la toxicité digestive de l'alcool, métabolisme glucidique (consommant la thiamine) augmenté par l'alcool, défaut du métabolisme de la thiamine (insuffisance hépato-cellulaire), incidence accrue des hypomagnésémies et autres pathologies favorisantes
- Divers (causes rares prises isolément mais totalisant près de 50% des cas dans leur ensemble) :
- régimes restrictifs ou déséquilibrés, anorexie, grossesse et allaitement, nutrition parentérale sans supplémentation, dénutrition, chirurgie gastro-entérologique, cancers, greffes, dialyses, syndromes d'immunodéficiences acquises, vomissements ou diarrhées persistants, insuffisance hépato-cellulaire, fièvres et situations hypercataboliques ou hypermétaboliques (hyperthyroïdie,...) prolongées, perfusions inadaptées, hypomagnésémies sévères, syndromes polyuriques et diurétiques, syndromes génétiques (anémie mégaloblastique thiamine dépendante, syndrome de dysfonction métabolique lié à la thiamine),...
- ces étiologies peuvent entraîner un syndrome de Wernicke et/ ou un béribéri seules, combinées ou sur un terrain d'alcoolisme chronique favorisant
- L'alcoolisme chronique en est la cause largement prédominante (présent dans > 50% des cas)
Implications pathologiques
Les conséquences pathologiques des carences et des troubles du métabolisme de la thiamine sont artificiellement (pour des raisons historiques) divisées en trois syndromes traités dans des chapitres spécifiques :
Certains états pathologiques entraînant des carences en thiamine entraînent bien sûr également leurs complications propres. Il n'y a par ailleurs pas de toxicité connue d'un excès de thiamine.
Prévention des carences
Au vu du taux médiocre de réponse thérapeutique des syndromes de Wernicke et du béribéri, de leur morbi-mortalité importante, de leur prévalence et de la relative innocuité d'une supplémentation vitaminique, cette dernière devrait être instaurée systématiquement pour :
- Supplémentation PO (ex : thiamine 300 mg/ jour) au long cours : tout éthylique chronique et patient malnutri, présentant une malabsorption, ayant subi une chirurgie bariatrique,...
- Supplémentation IV (500 à 1500 mg/ jour IV durant 3 à 5 jours) avant relais entéral :
- Tout patient éthylique chronique, malnutri ou présentant une malabsorption requérant une perfusion ou une renutrition. A discuter selon la situation pour certains patients à risques tels que ceux pris en charge pour un cancer
- Tout patient confus ou présentant des troubles de l'équilibre d'apparition (sub)-aiguë sans explication évidente
- Tout patient hospitalisé étant dans une situation hypermétabolique ou hypercatabolique prolongée (++ aux soins intensifs)
Cependant, comme souvent, l'essentiel des mesures de prévention dépassent le cadre strictement médical et relèvent d'une politique de santé publique : lutte contre l'alcoolisme, la malnutrition, la pauvreté et les régimes inadaptés. Au politique à prendre ses responsabilités.
Toxicité
La thiamine PO n'a pas de toxicité connue aux doses employées usuellement. En IV, des réactions anaphylactiques sont exceptionnellement décrites. A hautes doses ou chez des patients à risque, elle peut perturber l'équilibre glucidique.
Dosages en routine clinique
Les techniques de dosage de la thiamine circulante actuellement disponibles sont soit trop peu fiables (conditions de prélèvements et de transports stricts, la thiamine se dégradant rapidement), soit trop onéreuses et ne sont pas utilisées en routine clinique, le diagnostic de carence étant essentiellement posé sur base clinique et d'exclusion de diagnostics différentiels. Leur réalisation peut cependant se discuter avec certains laboratoires pour des études ou des situations cliniques très particulières.
Le dosage des métabolites du pyruvate est moins spécifique mais réalisable en routine et peut fournir un élément d'orientation. En cas de défaut de décarboxylation du pyruvate, on observe : acidose lactique, augmentation du pyruvate, rapport lactates/ pyruvate normal ou diminué, augmentation de l'alpha-cétoglutarate, augmentation de l'aluminium.
Bibliographie
Guilland JC, Vitamines hydrosolubles (I). Thiamine, riboflavine, niacine, acide pantothénique, vitamine B6 et biotine, Encyclopédie Médico-chirurgicale, Endocrinologie-Nutrition[10-546-A-10], Elsevier, Paris, 2012
Pazirandeh S et al., Overview of water-soluble vitamins, UpTodate, 2018
World Health Organization (WHO) and United Nations High Commissioner for Refugees (UNHCR), Thiamine deficiency and its prevention and control in major emergencies, WHO, 1999

